20. 痛いのはどうして嫌なの?— 脳内「不快神経」を同定 —
【要約】
痛みが不快であるのはよく知られていることですが、痛みが不快感を起こすメカニズムは分かっていませんでした。本研究では、不快な経験をした場所には近づかなくなるという動物の習性を利用し、分界条床核という脳部位でコルチコトロピン放出因子(CRF)とニューロペプチドY(NPY)という2種類の神経ペプチドが、痛みによる不快感の生起において逆の働きをすること、本脳部位の「2型神経細胞」とよばれる神経細胞の活動をCRFは促進し、NPYは抑制することを明らかにし、分界条床核「2型神経細胞」が、痛みによる不快感にかかわる「不快神経」であることを明らかにしました。
【背景】
私たちは痛みを不快に感じることで病気やけがに気づき医者や歯医者に行きます。動物も痛みを不快に感じることで危険な場所を回避したりすることができます。このように、痛みによる不快感は危険に対する防御や回避のために重要です。しかしながら、慢性痛では、警告信号の役割を果たした後でも痛みが続き、生活の質(QOL)を大きく損ないます。また、最近の研究では、痛みによる不快感が長く続くと、うつ病や不安障害などの精神疾患の引き金にもなり、また、そのような精神状態が痛みをさらに悪化させるという悪循環を生じさせることが報告されています。このことは、感情的な側面も考慮した疼痛治療の重要性と、その基盤となる不快感の神経機構解明の必要性を示唆しています。しかしながら、痛みが不快感を引き起こす脳内メカニズムについては分かっていませんでした。
【研究手法と研究成果】
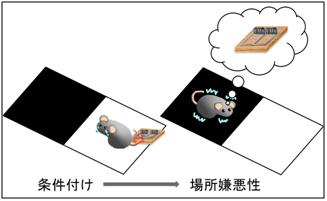
不快な経験をした場所には近づかなくなるという動物の習性を利用した「条件付け場所嫌悪性試験」(下図)という研究手法を用いて実験を行いました。実験動物(ラット)は、痛み刺激を与えられた場所に近づかなくなりますが、痛み刺激を与える10分前に分界条床核と呼ばれる脳部位にCRFの働きを抑制する薬物を投与しておくと、痛み刺激を与えた場所での滞在時間は、痛みを与える前後でほぼ同じでした(薬物処置をしない場合は、痛み刺激を与えた場所での滞在時間は短くなります)。同様に、分界条床核にNPYの働きを促進する薬物を投与した場合も、痛み刺激を与えた場所での滞在時間は、痛みを与える前後でほぼ同じでした。この結果は、CRFの働きの抑制およびNPYの働きの促進が、痛みによる不快感を抑制したことによると考えられます。
次に、1つ1つの神経細胞の活動状態を計測できる電気生理学的手法による解析を行いました。分界条床核の神経細胞は、1型から3型までの3種類に分類されることが知られていましたが、実験の結果、CRFとNPYはともに2型の神経細胞のみに働き、CRFは神経活動を亢進させ、NPYは神経活動を抑制することが明らかになりました。
以上の結果より、痛み刺激が加わると、脳内の分界条床核と呼ばれる部位で、CRFの働きが強まり、「2型神経細胞 = 不快神経」の活動を亢進させることで、不快感を引き起こしていること、NPYはCRFの働きを弱めて、不快感を抑制することが明らかになりました1)。
【考察と今後への期待】
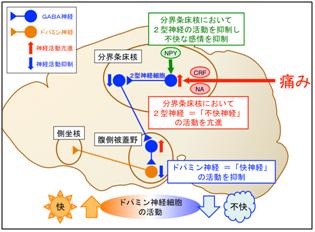
我々のグループは、これまでに、痛みによる分界条床核内ノルアドレナリン(NA)遊離亢進とそれにつづくβアドレナリン受容体活性化が痛みによる不快感の生起に重要であることを報告しています2)。また、DumontとWilliamsは、NAが分界条床核2型神経細胞(抑制性のGABA神経であると考えられています)に作用したのち、腹側被蓋野に投射する別のGABA神経を抑制することを報告しています3)。これらの知見を、今回の我々の研究結果、および、我々のグループが最近報告した分界条床核から腹側被蓋野への投射神経の神経化学的特徴4)と併せ考えると、1)痛みにより分界条床核内でCRFやNAの遊離が亢進し、2)「2型神経細胞 = 不快神経」の活動を亢進さることで、3)分界条床核から腹側被蓋野に投射するGABA神経を抑制し、4)腹側被蓋野内のGABA神経を脱抑制機構(当該神経を抑制している神経を抑制すること)により活性化させ、5)最終的に、腹側被蓋野内のドパミン神経の活動が抑制されるものと考えられます(下図)。腹側被蓋野ドパミン神経は、脳内報酬系と呼ばれる神経回路で「快神経」として働いており、この「ドパミン神経 = 快神経」が抑制されるために痛みが不快感を引き起こしたり、また、痛みがあると楽しいことが楽しく感じられなくなったり、やる気が出なくなったりするものと考えられます。
「分界条床核2型神経細胞 = 不快神経」は、痛みだけでなく、苦み・酸味や悪臭、暑さや寒さなどの感覚刺激、さらには、精神的なストレスにも反応して活動亢進し、不快な感情を引き起こすことが考えられます。また、この神経細胞の活動の異常がうつ病や不安障害などの精神疾患に関与している可能性が考えられ、疾患モデルにおける「分界条床核2型神経細胞 = 不快神経」活動の解析が、うつ病や不安障害のメカニズム解明と治療薬開発につながることが期待されます。
【文献】
- Ide, S., Hara, T., Ohno, A., Tamano, R., Koseki, K., Naka, T., Maruyama, C., Kaneda, K., Yoshioka, M., Minami, M. Opposing roles of corticotropin-releasing factor and neuropeptide Y within the dorsolateral bed nucleus of the stria terminalis in the negative affective component of pain in rats. J. Neurosci., 33: 5881-5894 (2013).
- Deyama, S., Katayama, T., Ohno, A., Nakagawa, T., Kaneko, S., Yamaguchi, T., Yoshioka, M. and Minami M. Activation of the -adrenoceptor–protein kinase A signaling pathway within the ventral bed nucleus of the stria terminalis mediates the negative affective component of pain in rats. J. Neurosci., 28: 7728-7736 (2008).
- Dumont, E.C., Williams, J.T. Noradrenaline triggers GABAA inhibition of bed nucleus of the stria terminalis neurons projecting to the ventral tegmental area. J. Neurosci., 24: 8198-8204 (2004).
- Kudo, T., Uchigashima, M., Miyazaki, T., Konno, K., Yamasaki, M., Yanagawa, Y., Minami, M., Watanabe, M. Three types of neurochemical projection from the bed nucleus of the stria terminalis to the ventral tegmental area in adult mice. J. Neurosci., 32: 18035-18046 (2012).
「神経化学トピックス」では、神経化学のトピックを一般の方にもわかりやすくご紹介します。
※なお、目次記載の所属は執筆当時の所属となっております。